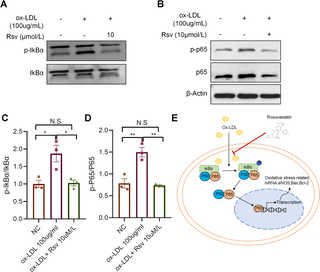
Pathofysiologie van atherosclerose: plaque van vorming tot ruptuur
Atherosclerose is een chronisch inflammatoir vasculair proces dat begint in de tweede levenstiende. Endotheeldisfunctie, LDL-oxidatie, macrofaaginfiltratie en gladde spiercelmigratje leiden tot plaquevorming. Plaqueruptuur of -erosie met superimposed trombus is het acute mechanisme achter hartinfarct en beroerte.
Kernbegrippen
- Endotheeldisfunctie
- Verlies van vasculaire homeostase door hypertensie, LDL, roken of hyperglykemie; initiatiefase van atherosclerose.
- Schuimcel (foam cell)
- Met oxLDL geladen macrofaag in de intimalaag; kernelement van het atherosclerotische atherroom.
- Fibrotische kap
- Laag glad spierweefsel en collageen over de lipidenkern; dunne kap = kwetsbare/instabiele plaque.
- Vulnerabele plaque
- Plaque met dunne fibrotische kap (<65 µm), grote lipidenkern en actieve inflammatie; hoog ruptuurrisico.
- Plaqueruptuur
- Scheuren van de fibrotische kap waardoor de lipidenkern in contact komt met bloed; activeert stollingscascade; leidt tot occlusieve trombus.
Van endotheeldisfunctie tot acuut coronair syndroom: stadia van atherosclerose
Initiatie: endotheeldisfunctie
Risicofactoren (LDL, hypertensie, roken, hyperglykemie) beschadigen het endotheel functioneel. Verminderde NO-productie, verhoogde adhesie-molecuulexpressie (ICAM-1, VCAM-1) en toegenomen permeabiliteit voor LDL initiëren het proces. LDL accumuleert subendotheliaal en raakt geoxideerd (oxLDL).
Vorming van het atheroom
OxLDL trekt monocyten aan die differentiëren tot macrofagen en via scavenger-receptoren massale hoeveelheden lipiden opnemen (schuimcellen). Gladde spiercellen migreren van de media naar de intima en produceren collageen. Inflammatoire cytokinen (IL-1β, TNF-α, IL-6) onderhouden het proces. Een lipidenkern met necrotisch centrum en neovascularisatie ontstaat.
Stabiele versus instabiele plaque
Stabiele plaque heeft een dikke fibrotische kap, kleine lipidenkern en weinig inflammatie. Instabiele (vulnerabele) plaque heeft een dunne kap (<65 µm), grote lipidenkern, actieve macrofaaginfiltratie en neovascularisatie. Matrix-metalloproteasen (MMPs) verzwakken de kap. Statines verbeteren de plaquesamenstelling: dikkere kap, kleinere lipidenkern.
Plaqueruptuur en trombus
Ruptuur van de fibrotische kap stelt de trombogene lipidenkern (tissue factor-rijk) bloot aan bloed. Plaatjesactivatie, stollingscascade en trombusvorming volgen. Of dit leidt tot een acuut coronair syndroom hangt af van de trombusmassa, het vaatlumen en de collateraalcirculatie. Plaque-erosie (zonder ruptuur) is de tweede mechanisme, met name bij jongere vrouwen.
Therapeutische implicaties
- LDL-verlaging stabiliseert en regrediert plaque (REVERSAL, SATURN-trials)
- Statines verminderen inflammatie onafhankelijk van LDL (JUPITER-trial: hsCRP-verlaging)
- Intensieve LDL-verlaging met PCSK9-remmers verlaagt ook plaquevolume (GLAGOV-trial)